EDTA er en kjemisk forbindelse som kan binde metallioner. Det brukes i en rekke sammenhenger, blant annet i behandling av akutte forgiftninger med enkelte tungmetaller, for eksempel bly, kobber og antimon.
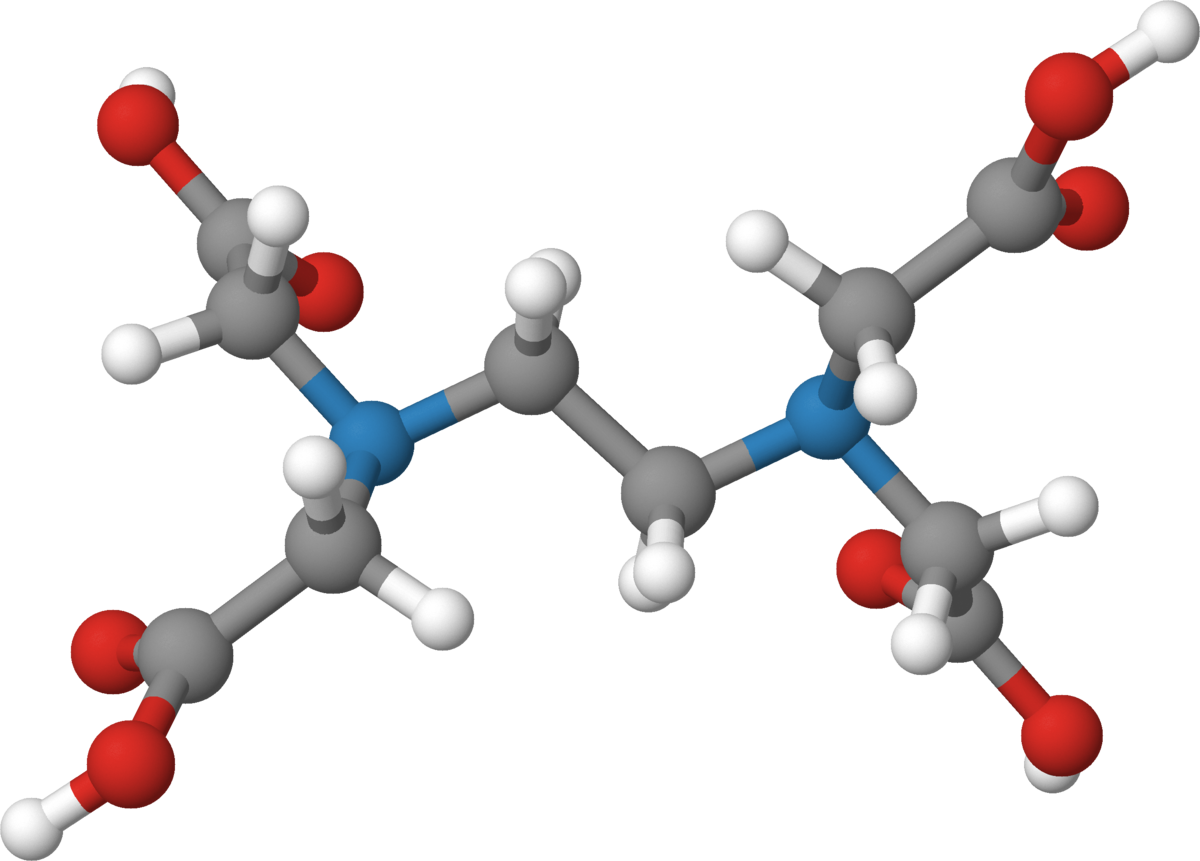
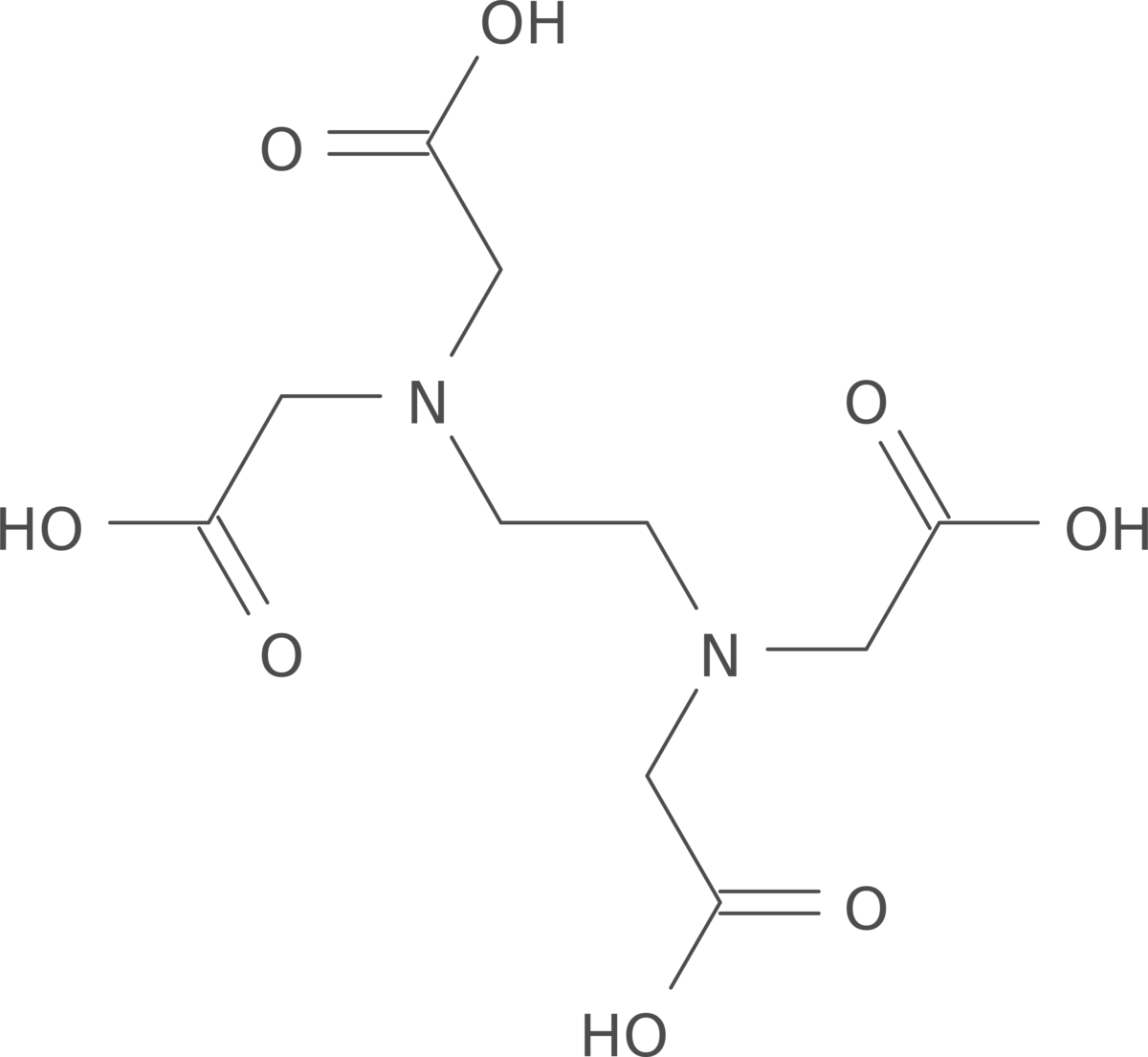
EDTA
Bruk
Behandling ved forgiftning
EDTA kan binde metallioner og danne ikke-ioniserte kompleksforbindelser (kelater). Disse forbindelsene er løselige og kan skilles ut gjennom nyrene.
EDTA binder også kalsiumioner, noe som kan ha meget farlige følger. Det blir derfor som regel gitt i form av en kalsium-EDTA-forbindelse, slik at konsentrasjonen av kalsium i blodet blir opprettholdt.
Tilsetning til blodprøver
EDTA kan tilsettes blodet ved blodprøvetaking for å hindre koagulasjon. EDTA binder da kalsiumionene som er nødvendige for å igangsette koagulasjonen. Når man fjerner blodcellene, får man da EDTA-plasma.
Hjelpestoff i legemidler
EDTA brukes som hjelpestoff i legemidler for å binde metallioner som ellers ville katalysere spaltingen av forskjellige legemidler.
Bløtgjøring av vann
Ettersom EDTA kan binde metaller, kan det brukes for å bløtgjøre hardt vann, binde spor av tungmetallioner i fett og oljer, eller dekontaminere radioaktive flater, samt i vaske- og renseoperasjoner av mange slag.
Kjemisk analyse
EDTA benyttes også i kjemiske analyser for å bestemme konsentrasjonen av metallioner, se titrering.
Kjemiske egenskaper
EDTA danner fargeløse krystaller som spaltes ved oppheting til 240 °C. Det løses lite i vann, men løser seg opp ved tilsetning av baser, for eksempel alkalihydroksider.
Som en firebasisk syre danner den mange salter, blant disse er dinatriumsaltet mest kjent. EDTA har kjemisk formel (HOOCCH2)2NCH2CH2N(CH2COOH)2.



Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.